日本NivoCUP试验结果公布:纳武利尤单抗治疗原发灶不明转移癌有效
原发灶不明转移癌 (carcinoma of unknown primary, CUP) ,是一种即使通过详细的病史,完善的辅助检查也不能确定原发位点,组织学确诊为转移癌的恶性肿瘤。CUP约占所有癌症的2%~5%,全世界发病率约为每 100,000人中5.3~19人,中位生存期为6-12 个月,预后较差。约80%的CUP患者无特异性治疗方法,通常使用经典的铂类化疗药物进行药物治疗。
最近,日本近畿大学医学部内科肿瘤学系通过对CUP进行的免疫组化 (IHC)和基因表达谱分析的结果显示,CUP可能与其他癌症类型相似,同样适用免疫检查点抑制剂(ICI)。
但由于目前ICI 对CUP疗效的数据有限,研究者们正在进行一项名为NivoCUP的多中心,开放标签,由医师主导的 II 期试验,以评估PD-1抗体纳武利尤单抗单药治疗 CUP的疗效和安全性。
《试验方法》
受试者为满足以下条件的CUP患者。*预后良好的CUP患者除外。
(1)具有可评估病灶(基于实体肿瘤疗效评价标准RECIST 1.1);
(2)ECOG体能状态 (PS评分) 为 0~ 1分;
(3)具有试验登记前 1 年内采集的肿瘤组织;
(4)无论先前是否接受过化疗。如先前接受过化疗,至少接受过1周期以上含铂类方案。
从2018 年 2月19日~ 2019 年8月9日,日本国内10个机构共计登记了56 例患者,其中先前接受过化疗者45 例,未接受治疗者11例。这些患者接受最多52个周期(2年)的纳武利尤单抗治疗(240 mg/间隔2周),直至出现疾病进展 (PD) 或不可接受的毒性。
主要终点:先前接受过化疗患者的客观缓解率(ORR)。
入组患者被分为“既往接受治疗组”和“未治疗组”。
★中位年龄:66.0岁(范围39-80岁),64.0岁(52-80岁);
★男性:17 例(37.8%),5例(45.5%);
★ECOG -PS评分 0/ 1:22.2%/77.8%,54.5%/45.5%;
★转移灶数量1/2/3以上:44.4%/17.8%/37.8%,54.5%/36.4%/9.1.%;
★既往接受治疗组先前治疗周期1/2/3以上:57.8% /20.0%/22.2%,多为卡铂+紫杉醇联合治疗方案。
★截至2020 年2月9日中位随访时间:既往接受治疗组8.4个月(范围0.1~21.6个月),未治疗组17.2个月(0.1~21.3个月)。既往接受治疗组中仍有7名患者 (15.6%) 在持续接受治疗。共有49例患者因疾病进展(PD)停止治疗,其中既往接受治疗组38名,未治疗组11名。
《试验结果》
1、既往接受治疗组客观缓解率22.2%,未治疗组18.2%,总体客观缓解率(ORR) 为 21.4%。
【既往接受治疗组】
★客观缓解率(ORR):22.2%(95%CI 11.2~37.1%)。
★完全缓解(CR)2例(4.4%);部分缓解(PR)8例(17.8 %)。
★中位缓解持续时间:12.4个月(范围 2.8~> 8.4个月)。
★中位无进展生存期(PFS):4.0个月(95% CI 1.9~5.8个月),6 个月时32%。
★中位总生存期(OS):15.9个月(8.4~21.5 个月),6个月时73%。
【未治疗组】
★客观缓解率(ORR):18.2%(95%CI 2.3~51.8%)。
★完全缓解(CR)1例;部分缓解(PR)1例(如表)。
★中位缓解持续时间:3.7个月(范围2.3~5.1个月)。
★中位无进展生存期(PFS) :2.8个月(95% CI 1.1~6.5个月),6个月时27%。
★中位总生存期(OS):未达到(95% CI 2.6个月未达到),6个月时73%。
总体客观缓解率(ORR) 为 21.4%。
(表1)基于 RECIST 1.1的最优综合疗效
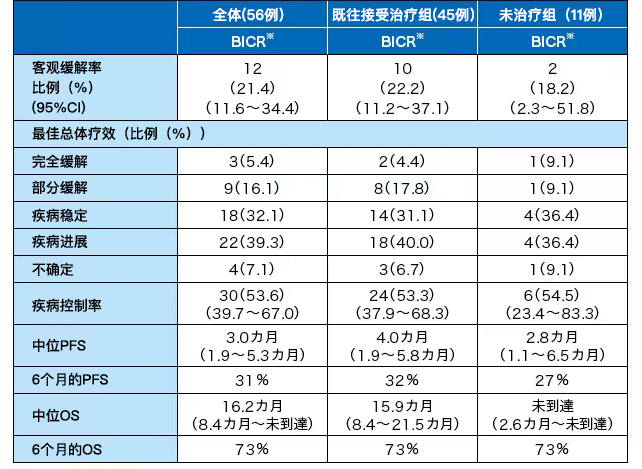
2、PD-L1≥1%,高TMB,MSI-High时疗效最佳
接下来,研究者们通过对受试者肿瘤的组织学类型,基因突变状态以及二代测序(NGS) 分析结果得出的推测原发灶,转移模式,ICI生物标志物PD-L1的表达,微卫星不稳定性(MSI)和肿瘤突变水平(TMB),对纳武利尤单抗的临床疗效进行了评估。
结果显示:
★按照组织类型进行的评估中,纳武利尤单抗的疗效没有差异。
★关于转移模式,仅有淋巴结转移病例(19 例)的 ORR,PFS和OS均优于其他病例(37 例)。
★根据NGS分析结果,对推测原发灶治疗相对敏感的癌症类型(大肠癌、乳腺癌、卵巢癌、非小细胞肺癌等)与其他癌种,预后和纳武利尤单抗疗效没有明显差异。
★PD-L1表达状态评估55例(基于免疫组化IHC)。
PD-L1 TPS 或CPS ≥ 1% 的患者分别为30.9%和78.2%。
PD-L1 TPS ≥1%、≥10%,≥50%的患者中,ORR分别为 41.2%,46.7% 和 57.1%;
PD-L1 TPS<1%的患者仅为13.2%。
PD-L1 CPS ≥ 1%、≥10%、≥50% 患者的ORR分别为 27.9%,31.3% 和 40.0%,而 PD-L1 TPS<1%的病例为0%。
★TMB评估50例,中位数7.75 mut/Mb。
高于中位TMB患者的ORR,PFS和OS均优于低于中位TMB的患者。(如表2)。
(表2)高于中位TMB /低于中位TMB的预后
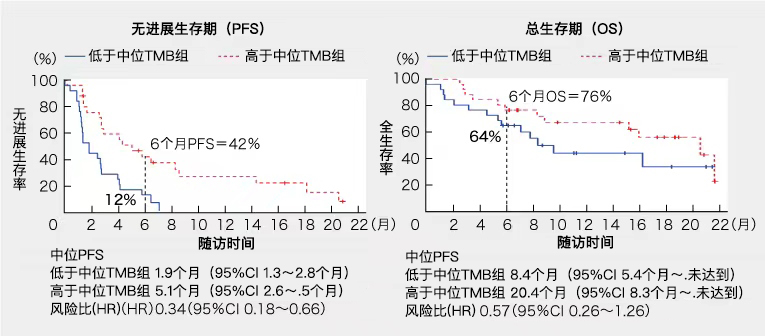
★MSI评估42例,其中MSI-high 2例(4.8%)。这两例的推测原发灶分别为胰腺腺癌和肾细胞癌,TMB值分别为23.4 mut/Mb和25.1 mut/Mb。数据统计截止时此2例均显示部分缓解(PR),并继续接受治疗。
既往接受治疗组的43 名微卫星稳定性 (MSS)患者中,ORR为 18.6%(95% CI 8.4~33.4%)。研究者认为:“即使在MSS 病例中,纳武利尤单抗仍可有效改善预后。”
★最常见的基因突变是TP53,其次是EGFR和KRAS。这些基因突变的存在与否与纳武利尤单抗的疗效无关。
3、不良事件(AE)无加剧
试验观察到不良反应53例。其中3/4级为34例(60.7%),重度不良反应27例(48.2%),其中 4 例因此停用纳武利尤单抗。无治疗相关的死亡。
最常见的AE为便秘(13 例,23.2%),贫血(10 例,17.9%),腹泻(10 例,17.9%),甲状腺功能减退(9 例,16.1%),皮疹(9 例,16.1 %)。
免疫相关不良反应32 例 (57.1%),但大多为1/2级。3/4级共4例,其中急性肾损伤2例,肝炎和皮疹各1例。
从这些结果来看,“纳武利尤单抗对 CUP患者的临床治疗有效,可能是 CUP患者的一个新治疗选择。”
《试验结论》
① 推测:免疫检查点抑制剂(ICI)可能对CUP长期有效。
② PD-L1表达,MSI和TMB可能对纳武利尤单抗的治疗效果有预测作用。
* TPS-Tumor Proportion Score:肿瘤比例评分,肿瘤细胞中PD-L1表达阳性细胞的百分比.
* CPS-Combined Positive Score综合阳性评分,肿瘤细胞和肿瘤浸润性免疫细胞(淋巴细胞、巨噬细胞)在“肿瘤细胞总数”中 PD-L1 表达阳性细胞的百分比.


