胃肠道神经内分泌癌的综合基因组分析揭示了发病和发展的机制--大阪大学等
共115例神经内分泌肿瘤和神经内分泌癌的综合基因组分析
大阪大学12月9日宣布,通过使用来自日本、美国和欧洲的样本进行全基因组和其他分析,阐明了胃肠道神经内分泌癌(NEC)的致癌机制,这是一种难治的癌症。 这项研究是由该大学医学研究生院和国家癌症中心研究所基因组医学部主任谷内田新一教授(癌症基因组信息学)领导的一个国际研究小组进行的。 该研究结果已发表在美国癌症研究协会的期刊《癌症发现》上。
神经内分泌肿瘤(NENs)是一种罕见的疾病,其免疫组化染色对神经内分泌标记物(如突触蛋白和色氨酸A)呈阳性。 根据2010年WHO的分类,NENs根据细胞增殖的程度和有丝分裂的数目被分为G1、G2或G3。 然而,由于一些G3的预后相对较好,而另一些则非常差,2019年的WHO分类首先根据组织病理学将NENs分为神经内分泌肿瘤(NETs)和神经内分泌癌(NECs)。 根据组织病理学,NECs被分为小细胞型和大细胞型。 小细胞型在组织学上与小细胞肺癌相似。
由于NETs通常是通过手术治愈的,因此利用手术后的残留标本进行研究,并确定了几个致病基因,包括MEN1。 另一方面,NEC极其罕见,而且在诊断时往往伴有远处转移,因此很少有患者适合做手术,而获得研究样本的困难也阻碍了大规模的综合基因组分析。 然而,研究小组对胃肠道NETs和NECs(共115例)进行了全面的基因组分析(全基因组分析、全外显子组分析、全转录组分析(RNA-seq)、甲基化分析和ATAC-seq分析),并证明两种疾病的发病机制完全不同。 我们已经证明,它们是两种不同的疾病。
胰腺来源的NEC可分为导管型和针叶型,它们可能有不同的细胞来源
NECs按器官分为胰腺和非胰腺胃肠道来源进行分析。 组织病理学是相似的,但基因组畸变显示了相似性和差异性。 他们还发现,胰腺来源的NECs以TP53和RB1基因的异常为特征,可分为 "导管型 "和 "针叶型"。
前者有KRAS基因的突变和胰腺导管细胞标记基因(SPP1和CFTR)的表达升高。 后者没有KRAS突变,并有一个胰腺细胞标记基因(PTF1A)的高表达。 管状型和针状型NECs之间的差异可能是由于它们在胰腺中的不同细胞起源所致。 胰管型胰腺癌可能有一个共同的起源细胞,因为存在KRAS突变,这在常规胰腺癌中也是高发的,但缺乏常规胰腺癌中的大部分CDKN2A和SMAD4基因异常。有人认为,疾病的方向可能分为正常型胰腺癌和导管型NEC。
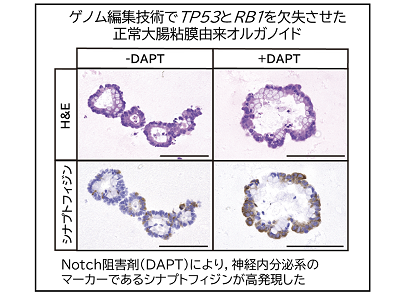
非胰腺胃肠道来源的NECs的特点是TP53和RB1基因或TP53和CCNE1或MYC基因的异常(相互排斥),以及大量的结构多态性。 非胰腺胃肠道来源的NECs也以Notch基因家族的异常为特征。 事实上,我们用来自结肠粘膜的器官验证了抑制Notch信号会诱导突触蛋白阳性细胞,这是一种神经内分泌的标记。
与非胰腺胃肠道来源的NECs相比,胰腺来源的NECs的五年生存率明显较低。 此外,胃部NEC和结直肠NEC各发现一例是由病毒感染引起的(胃部NEC:梅克尔细胞多瘤病毒,结直肠NEC:人类乳头瘤病毒)。 在这种病毒性致癌中,没有观察到TP53和RB1基因的异常。
由于启动子甲基化,转录因子SOX2/ASCL1在NEC高度表达
研究人员还发现,NECs的一个主要特征是SOX2和ASCL1的高表达,这两个转录因子能调节神经内分泌的分化,而这是由于每个基因的启动子区域被甲基化了。 一般来说,启动子区域的去甲基化会导致基因表达的增加,但最近也有相反的报道。 此外,ATAC-seq分析显示,在SOX2高表达的NECs中,SOX2周围区域具有开放的染色质结构,即基因转录得到促进。
研究结果表明,NEC可能会导致腺癌或鳞状细胞癌。
在NECs的病理中还可以观察到普通腺癌和鳞状细胞癌,当其成分超过30%时,被称为神经内分泌-非神经内分泌混合性肿瘤(MiNEN)。 到目前为止,大多数MiNENs被认为是腺癌或鳞状细胞癌,分化成神经内分泌NECs。 然而,在这项研究中,通过比较两种成分的基因组畸变,研究人员观察到的结果表明,NECs可能积累了额外的基因畸变,导致腺癌和鳞状细胞癌。
NETs表现出与NEC完全不同的发病机制
研究人员还证明,NETs的发展机制与NEC完全不同,在NEC的大多数病例中没有观察到RB1基因的异常情况。 NETs没有在大多数NECs中观察到的RB1基因异常,并且比NECs有更少的基因突变,有突变的主要基因是MEN1、DAXX和VHL基因。 有趣的是,大约40%的胰腺NETs发生了大量的染色体水平缺失(1、2、3、6、8、10、11、15、16、21和22号染色体),这些病例中大约三分之二有MEN1基因的突变。
MEN1基因编码一种叫做Menin的蛋白质,已知它参与了染色体结构的维护和DNA修复。 这些发现表明,MEN1突变可能在细胞分裂过程中破坏了染色体分离机制的稳定性,导致了这种现象。
此外,他们发现,当NETs从G1和G2发展到G3时,会积累基因异常,如TP53和CDKN2A。
界定新的亚组,促进药物重新定位和新药开发
该研究结果在全基因组水平上阐明了胃肠道NEC这一罕见的难治性癌症的发生和发展机制。NEC的基因组异常与同一器官来源的常规癌症(腺癌和鳞状细胞癌)不同,而且很少有基因异常可以被现有的药物如分子靶向药物所针对。 这也是一种目前难以治愈的癌症。 该研究小组说:"通过详细分析复杂多样的发病机制,并根据致癌机制定义新的亚组,我们希望能促进正在开发的分子靶向药物的药物重新定位和新药开发。


