首例iPS细胞衍生的NK细胞疗法用于卵巢癌的P1研究 - CiRA等
iCAR-ILC-N101腹腔内给药的安全性和耐受性研究
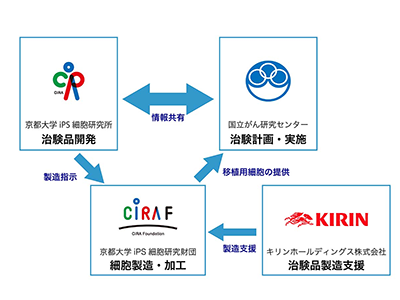
京都大学iPS细胞研究所(CiRA)于11月11日宣布,研究腹腔注射抗Glypican 3 (GPC3)-CAR表达的iPS细胞衍生的ILC/NK细胞(开发名称:iCAR-ILC-N101)的安全性和耐受性的I期临床试验的第一个受试者被注射了 这项研究是在该研究所的金李医院进行的。 这项研究是由Arata Kaneko教授和他的研究小组在国立癌症中心医院东区进行的。
使用CAR转基因T细胞(CAR-T细胞)和CAR转基因NK细胞(CAR-NK)的癌症免疫疗法已被证明对一些癌症有显著的治疗效果。 Arata Kaneko教授和她的研究小组一直在开发iPS细胞介导的抗原特异性再生T细胞和再生NK细胞制剂。 特别是,使用HLA同源iPS细胞的再生免疫细胞可用于多个病人,并有望获得稳定的供应。 它们还可以通过基因组编辑来增强免疫细胞的功能,避免细胞衰竭。
该研究小组专注于GPC3,一种具有极高癌症特异性的蛋白质。 该研究小组专注于GPC3,这是一种高度癌症特异性的蛋白质,并将识别GPC3的CAR基因引入iPS细胞(QHJI01s04),该细胞与日本人口中最常见的HLA同源,并将其分化为NK细胞(开发名称:iCAR-ILC-N101)。iCAR-ILC-N101计划用于临床试验,以治疗经常表达GPC3的卵巢透明细胞癌。 该试验于2021年4月在国家癌症中心东院开始,并在9月进行了第一次细胞移植。
表达GPC3的晚期复发性卵巢透明细胞癌患者无法手术并伴有腹膜播散性疾病
该研究是在表达GPC3的无法手术的晚期复发性卵巢透明细胞癌患者中进行的,并伴有腹膜播散的疾病。 对于细胞移植,iCAR-ILC-N101的剂量为1 x 106个细胞/kg,每周一次,最多可重复四次经皮进入腹腔。 根据剂量依赖性毒性的出现,最小剂量将是0.5 x 106个细胞/公斤,22天内最多4次,最大剂量将是3 x 106个细胞/公斤,22天内最多4次。
计划患者人数为6至18人,研究期限为2021年4月12日至2024年3月31日。


