基因编辑的T细胞如何对抗癌症
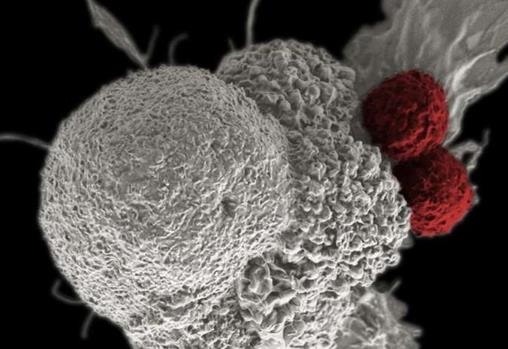
伪彩色扫描电子显微照片显示两个T细胞(红色)攻击癌细胞(白色)。研究人员正在通过编辑T细胞内的基因来创造更强大的癌症治疗方法。图片来源:Rita Elena Serda,美国贝勒医学院邓肯综合癌症中心,美国国家癌症研究所,美国国立卫生研究院,CC BY-NC
在美国,基因编辑首次用于治疗三名晚期癌症得患者,并在1期临床试验中显示出令人鼓舞的早期结果。到目前为止,该治疗方法似乎是安全的,并且有望很快获得更多结果。
在这种治疗中,将患者自身的免疫细胞从体内提取,接受训练以识别特定的癌细胞,然后最终将其注入患者体内,使其繁殖并破坏它们。与直接杀死癌细胞的化学疗法或放射疗法不同,免疫疗法激活人体自身的免疫系统来发挥作用。这个团队使用了一种叫做CRISPR的基因编辑工具来改变免疫细胞,将它们变成训练有素的士兵来定位和杀死癌细胞。通过使用这种技术,研究小组希望开发一种副作用最小的更有效的免疫疗法。
训练免疫细胞以发现并杀死癌症
癌症药物试验的这些杀死肿瘤细胞的第一步是从癌症患者的血液中分离出T细胞(一种与病原体和癌细胞对抗的白细胞)。该研究招募了两名患有晚期多发性骨髓瘤的患者和一名患有类固醇/圆形细胞脂肪肉瘤的患者。
为了武装T细胞并增强其抗肿瘤能力而又不损害正常细胞,科学家将T细胞进行了基因改造(禁用了三个基因,并添加了一个基因),然后再将其返回给患者。
这些缺失的基因中的前两个编码T细胞受体,T细胞受体是在T细胞表面上发现的蛋白质,可以识别并结合癌细胞上称为抗原的特定分子。当这些经过改造的T细胞与这些抗原结合时,它使它们能够攻击并直接杀死癌细胞。但是问题是单个T细胞可以识别体内多种不同的抗原,从而使它们不太专注于寻找癌细胞。通过消除这两个基因,T细胞不太可能攻击错误的靶标或宿主,这种现象称为自身免疫,
此外,他们破坏了第三个基因,称为程序性细胞死亡蛋白1,该基因减慢了免疫反应。禁用程序性细胞死亡蛋白1基因可提高T细胞的效率。
这些细胞转化的最后一步是添加一个基因,该基因产生一个新的T细胞受体,该受体识别并捕获癌细胞上称为NY-ESO-1的特定标记。现在删除了三个基因,又添加了一个基因,这些T细胞就可以对抗癌症了。
通过用CRISPR剪切掉三个基因并添加一个新的基因来修饰T细胞后,免疫细胞在定位和杀死癌细胞方面变得更好
CRISPR在这项临床试验中
那么,这个团队如何精确地编辑T细胞?他们利用了CRISPR / Cas9基因编辑技术,该技术使用了两个组件:一个可以找到并结合目标基因位点的CRISPR向导分子,一个分子剪Cas9剪切DNA,最终使基因失活。
该团队使用电穿孔技术,该技术可在细胞膜上产生临时孔,从而将Cas9蛋白与靶向分子的靶向分子一起传递给数百万个T细胞中的三个感兴趣的基因。
在使用CRISPR破坏了这三个基因后,研究小组使用了一种安全的,失活的病毒将一个基因传递给T细胞,从而使其能够识别癌症特异性标记物NY-ESO-1。从数百万个细胞中去除这些基因,然后让T细胞在培养皿中体外繁殖成数十亿个细胞,可能需要几天到几周的时间。
在注射CRISPR修饰的T细胞前四天,研究小组为三名患者中的每人提供了几剂化疗药物,以耗尽体内现有的白细胞。
最后,每公斤体重约有1亿个修饰的T细胞作为单次输注被注入患者体内。
CRISPR的光明前景
该小组在注射T细胞后的头28天连续监测患者。然后,他们每月随访六个月。之后,每三个月监测一次不良事件,即免疫反应。T细胞疗法通常与各种副作用有关,例如发烧,肌肉疼痛,头痛,意识错乱,癫痫发作,低血压,出血性疾病和多器官功能障碍,研究小组没有发现任何患者出现中毒的迹象,这令人兴奋。
但是第一位患有晚期多发性骨髓瘤的患者在60天后仍继续出现肿瘤。尽管对于第一位患者而言治疗似乎并不那么成功,但1期临床试验主要是为了测试安全性,该小组报告对任何患者均无毒性。
使用串行CT扫描监测第二例患有晚期粘液样/圆形细胞脂肪肉瘤的患者,并且在90天后似乎稳定。第三位多发性骨髓瘤患者最近开始试验,尚无结果。这项基于CRISPR基因编辑技术的新疗法对癌症患者没有严重的毒性问题,这是向临床广泛应用迈出的重要一步。


