结直肠癌首个无化疗靶向方案III期临床获得成功
今年6月,辉瑞宣布以110亿美元收购Array。近日,该公司公布了结直肠癌III期临床研究BEACON CRC的数据。该研究在既往已接受一种或两种疗法的晚期BRAF V600E突变转移性结直肠癌(mCRC)患者中开展,评估了Braftovi(encorafenib,BRAF抑制剂)联合Mektovi(binimetinib,MEK抑制剂)及Erbitux(cetuximab,抗EGFR抗体)三联疗法的疗效和安全性。

值得一提的是,BEACON CRC研究是评估BRAF/MEK联合靶向疗法治疗BRAF V600E突变型mCRC的第一个也是唯一一个III期研究。来自该研究的强劲疗效证据,支持了Braftovi三联方案作为BRAF突变mCRC患者第一种无化疗靶向治疗方案的潜力。Array公司计划在2019年下半年向监管机构提交Braftovi三联方案的监管申请文件。
德克萨斯大学安德森癌症中心癌症医学部胃肠道医学肿瘤学系副教授Scott Kopetz博士表示:“令人非常振奋的是,来自BEACON CRC研究的结果有望改变临床实践,与BRAF V600E突变mCRC患者的现有标准治疗方案相比,该研究的结果具有显著改善。这些数据为支持Braftovi三联方案作为该患者群体潜在新治疗标准提供了证据,目前该类患者的治疗选择有限。”
具体结果为:该研究达到了主要终点:与Erbitux+含伊立替康方案治疗的对照组相比,Braftovi三联方案治疗组总生存期(中位OS:9.0个月 vs 5.4个月,HR=0.52[95%CI:0.39-0.70],p<0.0001)和客观缓解率(ORR:26.1% vs 1.9%,p<0.0001)均表现出统计学意义的显著改善。此外,Braftovi三联方案治疗组无进展生存期也表现出统计学意义的显著改善(中位PFS:4.3个月 vs 1.5个月,HR=0.38[95%CI:0.29-0.49],p<0.0001)。
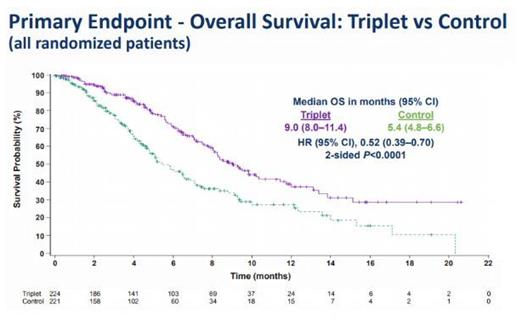
该研究在次要终点方面也表现出改善:与对照组相比,Braftovi+Erbitux二联方案治疗组OS(中位数:8.4个月 vs 5.4个月,HR=0.60,95%CI:0.45-0.79,p=0.0003)和ORR(20.4% vs 1.9%,p<0.0001)也表现出统计学意义的显著改善。此外,Braftovi+Erbitux二联方案组PFS也表现出统计学意义的显著改善(中位PFS:4.2个月 vs 1.5个月,HR=0.40,95%CI:0.31-0.52,p<0.0001)。
描述性比较分析显示,与Braftovi二联方案相比,Braftovi三联方案在包括ORR、OS在内的所有终点均呈现积极趋势(HR=0.79,95%CI:0.59-1.06)。
该研究中,对照组与以往报道的研究和疗效终点的历史数据一致,这强调了BRAF突变mCRC患者在当前可用的药物方案中通常预后不良。目前,还没有获FDA批准专门针对这类高医疗需求群体的治疗方案。BRAF突变发生在15%的mCRC患者中,V600E是最常见的突变。
安全性方面,Braftovi三联方案和二联方案的耐受性良好,无意外毒性,安全性与以往报道的每种方案的经验及MEK、BRAF和EGFR疗法一致。
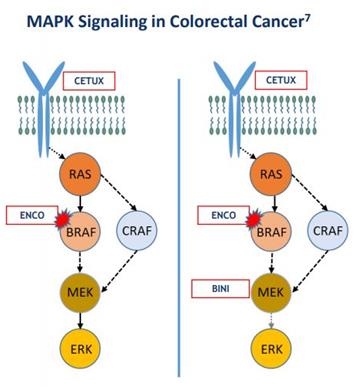
MEK和BRAF是MAPK信号通路(RAS-RAF-MEK-ERK)中的关键蛋白激酶。研究表明,这一通路调节了包括细胞增殖、分化、存活、血管生成在内的多种关键细胞活动。在许多癌症中,如黑色素瘤、结直肠癌和甲状腺癌,这一信号通路中的蛋白质已被证实异常激活。
Braftovi是一种BRAF抑制剂,Mektovi则是一种MEK抑制剂,这2种药物均靶向该信号通路中的关键酶。去年6月,Braftovi+Mektovi组合已获美国FDA批准,成为治疗BRAF突变黑色素瘤在III期临床中生存期超过30个月的首个靶向疗法,代表着BRAF突变黑色素瘤的一种新的临床护理保准。


