日本胃癌专家详解: 全球首款靶向CLDN18.2的佐妥昔单抗(Zolbetuximab)的有效性
2024年3月,日本厚生劳动省批准了抗CLDN18.2抗体zolbetuximab的新药上市申请。该药将成为HER2阴性、不可切除的晚期/复发性胃癌的新治疗选择,预计最早将于六月开始临床实施。日本厚生劳动省的批准使VYLOY成为全球目前首个且唯一获批的CLDN18.2靶向疗法。
关于该药物,已经有许多评论,以下将由日本东邦大学研究生院胃肠外科和临床肿瘤学教授-岛田英昭将根据迄今为止发表的主要论文,总结实践中的期望和挑战。

作为胃癌治疗靶点而备受关注的CLDN18.2到底是什么?
Claudin(CLDN)18.2 是紧密连接蛋白家族Claudin 18 的亚型,是一种高度特异性的恶性肿瘤生物标志物,在正常组织中很少表达(图1)。CLDN18.2参与胃癌/食管胃结合部癌、乳腺癌、结直肠癌、肝癌、头颈癌、非小细胞肺癌等肿瘤细胞的增殖和分化。尤其是作为胃癌的治疗靶分子而受到关注。
图1. CLDN18.2染色的胃食管癌标本
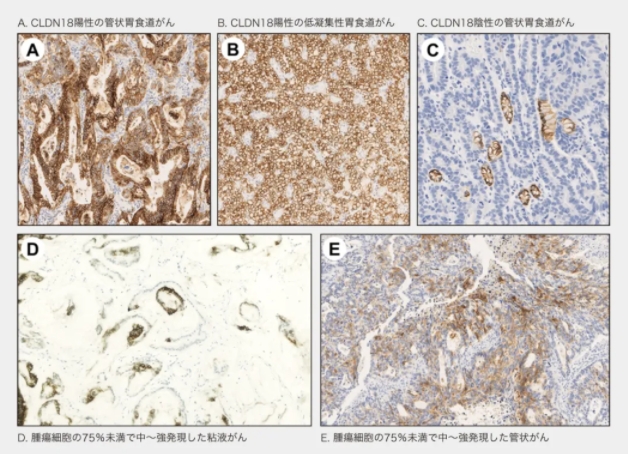
(Pathol Res Pract 2023; 248: 154699)
在Baek等研究者们对367例胃癌患者进行的研究中,免疫组化染色结果显示,273例患者(74.4%)有CLDN18.2表达。根据预先指定的标准,108例患者(29.4%)被确定为CLDN18.2阳性。弥漫性和HER2阳性患者中CLDN18.2的表达率较高,但与预后无关(Anticancer Res 2019; 39: 6973-6979)。
在Tao等研究这们对426名胃癌患者进行的研究中,CLDN18.2表达与HER2、p53、三叶因子(TFF)2、肿瘤免疫浸润、PD-1通路、细胞周期和Wnt信号通路相关。(Pathol Res Pract 2023; 248: 154699)。
在Dai等研究者们对43例胃癌/食管胃交界癌患者的腹水标本和相应的活检/切除标本进行的免疫组织化学染色显示,当阳性定义为≥40%的肿瘤细胞中有中度到强表达时,在24份(55.8%)组织标本和22份(51.2%)腹水标本中观察到CLDN18.2表达。如果将CLDN18.2阳性的临界值设定为40%时,腹水标本和组织标本之间显示出83.7%的高度吻合率(Cancer Cytopathol 2023; 131: 365-372)。
两项临床试验证明了其优越性
【SPOTLIGHT试验】
是一项III期临床试验,旨在检验在奥沙利铂+左亚叶酸+氟尿嘧啶(mFOLFOX6)疗法中添加佐妥昔单抗(zolbetuximab)的效果。在对565名CLDN18.2阳性(肿瘤细胞75%+的中重度表达)的不可切除晚期/复发性胃癌患者研究后发现,中位无进展生存期(PFS)具有显著的优势。mFOLFOX6+安慰剂组为8.67个月,mFOLFOX6+佐妥昔单抗组则为10.61个月。(风险比HR0.75,95% CI 0.60-0.94,P = 0.0066)。mFOLFOX6 +佐妥昔单抗组最常见的不良事件是恶心、呕吐和食欲下降。此外在亚组分析中,在日本人、亚洲人和胃切除术后患者中观察到良好的HR(Lancet 2023; 401: 1655-1668)。
【GLOW试验】
是一项III期临床试验,旨在检查在卡培他滨+奥沙利铂(CAPOX)治疗基础上添加佐妥昔单抗的效果。与SPOTLIGHT研究类似,CLDN18.2阳性被定义为肿瘤细胞75%+,CLDN18.2中度至强表达。在对507名患者的研究中,CAPOX+佐妥昔单抗组的中位PFS显着优于CAPOX加安慰剂组的6.80个月,为8.21个月。( HR=0.687,95 % CI 0.544~0.866,P = 0.0007)。中位总生存期OS在CAPOX +佐妥昔单抗组为14.39个月,而安慰剂组则只有12.61个月。(HR= 0.771、95 % CI 0.615~0.965,P = 0.0118,图2)。两组间不良事件发生率无显着差异。
图2: GLOW 研究中显示的Zolbetuximab的OS
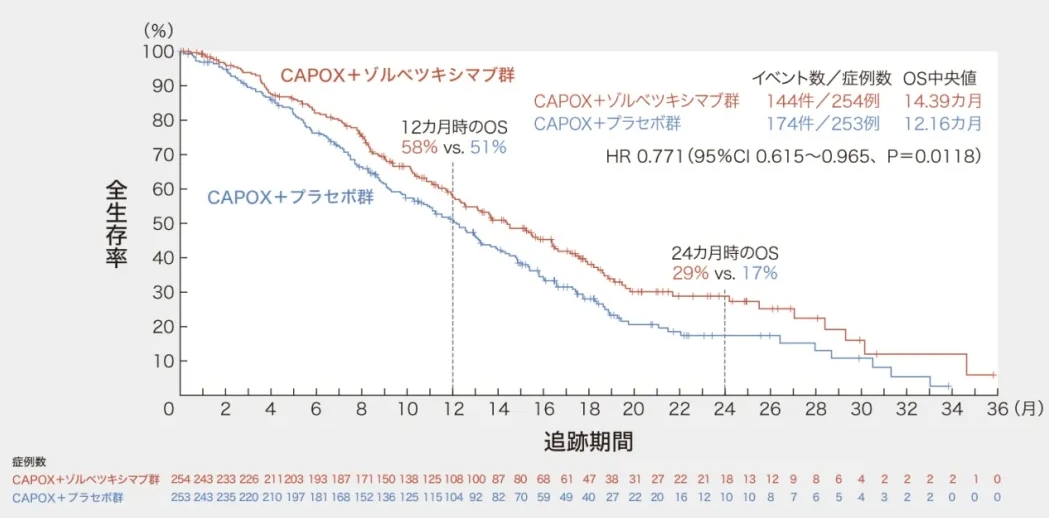
(Nat Med 2023; 29; 2133-2141)
尽管GLOW研究中的日本患者数量较少,只有51例,但针对日本患者的亚组分析显示OS的HR非常有利,为0.425(95% CI 0.195~0.924)。关于OS,HR为0.678(0.512~ 0.898),即使在整个亚洲患者中也表现良好,结果表明该药物有望对日本患者有效。另外,虽然胃切除术后的病例数较少(150例),但HR为0.632(0.408~0.982),这是一个不错的结果。
另一方面,与SPOTLIGHT研究类似,对不良事件的担忧包括恶心和呕吐的高发生率。特别是在临床实践中向患者解释这一情况时,应牢记66%的患者会发生呕吐的事实。据推测,胃切除术后病例的OS HR 较好可能是由于呕吐较少所致(Nat Med 2023; 29; 2133-2141)。
岛田英昭教授认为:在HER2阴性胃癌一线治疗中佐妥昔单抗可能优于纳武单抗
随着佐妥昔单抗的出现,在已确定无法切除的晚期/复发性胃癌的一线治疗中,我们将进行四类生物标志物的表达检查:HER2、CPS、CLDN18.2和微卫星不稳定性(MSI),以确定治疗方案。目前,HER2阳性胃癌的治疗以含曲妥珠单抗的方案开始,但对于HER2阴性胃癌,可能根据CPS和CLDN18.2的表达状态来选择免疫检查点抑制剂或佐妥昔单抗。如果每项检测均呈阳性,则应优先考虑针对阳性的治疗,这无争议。然后在应该根据具体情况及各种背景因素来做选择。
此外,当我们检查晚期胃癌患者中CLDN18.2的表达与其他生物标志物之间的关系时发现,CLDN18.2阳性组中CPS 5以上的频率低于CLDN18.2阴性组约10个百分点。尽管这并不显着(41.9% vs. 51.5%,P=0.122,ESMO Open 2023;8:100762)。三线治疗中还可以选择使用抗PD-1抗体nivolumab,而且即使单独使用也有望获得良好的治疗效果。因此一线治疗中可优先考虑使用佐妥昔单抗。


