ESMO2022 乳腺癌研究汇总
今年的欧洲肿瘤内科学会(ESMO)公布了众多重要的研究结果,而这些结果将改变当前肿瘤的治疗格局,会对未来的治疗方向产生重大影响。其中,关于晚期乳腺癌就有很多令人期待的研究成果。以下,由日本国立癌症研究中心中央病院的医生下井辰徳为我们做个乳腺癌最新研究的汇总及解析。

日本国立癌症研究中心中央病院
肿瘤内科主任医师
下井 辰徳
① TROPiCS-02 研究:sacituzumab govitecan 显著延长OS
【sacituzumab govitecan】
中文通用名: 戈沙妥珠单抗 or赛妥珠单抗
这是一款新型抗体偶联药物(ADC),由靶向TROP-2的抗体与化疗药物伊利替康(Irinotecan)的活性代谢物SN-38连接构成的抗体偶联药物(ADC)。它能够通过与TROP-2蛋白相结合,将化疗药伊利替康的活性代谢物SN-38递送到癌细胞内部。
ASCENT 试验是一项随机对照的 III 期临床试验,针对既往接受过至少2种化疗的转移性/复发性三阴性乳腺癌(TNBC)。该药物因能够提高无进展生存期 (PFS)和总生存期(OS),已被FDA批准用于治疗三阴性乳腺癌(TNBC)。
目前正在进行的TROPiCS-02 研究 (ClinicalTrials.gov, ID: NCT03901339) 也是一项随机对照的 III 期试验。该试验评估比较了 sacituzumab govitecan (SG组)和医师选择的治疗(TPC组)对内分泌治疗耐药的 HR +/HER2-晚期乳腺癌患者的疗效。
根据2022 年 ASCO 年会上报告的结果:
★无进展生存期(PFS)
SG 组:5.5 个月
TPC 组:4.0 个月
⇒SG 组的中位 PFS 优于 TPC 组(HR=0.66,95% CI: 0.53-0.83,p = 0.0003)
★6 个月 PFS 率
SG 组:46%
TPC 组:30%,
★12 个月 PFS率
SG 组:21%
TPC 组:7%,
⇒两者都有利于 SG 组。
总生存期(OS),在第一次中期分析中无统计学上的明显差异。SG组中性粒细胞减少的不良事件为51%,腹泻为9%,但导致治疗中止的严重不良事件SG组为6%,TPC组为4%,差异不大。
而此次ESMO 上公布的结果即为第二次中期分析结果。
★中位总生存期(OS)
SG 组:14.4 个月,
TPC 组:11.2 个月
⇒SG 组的 OS 明显更好(HR= 0.79,95% CI: 0.65-0.96,p=0.020)。
★12 个月的 OS 率
SG 组:61%
TPC 组:47%
★反应率
SG 组: 21%,
TPC 组:14%(p=0.035)
⇒SG 组明显更好。
Sacituzumab govitecan 是少数几种治疗 HR +/HER2 -晚期乳腺癌的药物之一,与其他抗癌药物相比,除了 PFS 外,OS 也有所改善。因此,该药将被定位为HR+/HER2-晚期乳腺癌的标准治疗方法之一。此外,一些 HER2 低表达的 HR+/HER2-乳腺癌病例与 Trastuzumab deruxtecan(德喜曲妥珠单抗/DS-8201)的病例重叠(Destiny Breast 04 研究)。未来也会考虑这两种药物的定位。
②MONARCH-3 研究:abemaciclib表现良好
【Abemaciclib】
中文通用名:阿贝西利
阿贝西利是一种 CDK4/6 抑制剂,在 HR +/HER2-中表现出显著改善,被批准与非甾体芳香酶抑制剂(NSAI)联合用作绝经后晚期乳腺癌患者的一线内分泌治疗。该研究的次要终点 OS 的第二次中期分析已经发表。
★中位 OS(中位随访时间5.8 年)
在总体人群(ITT 人群)中,
阿贝西利+NSAI :67.1 个月,
安慰剂+NSAI : 54.5 个月
⇒未超过用于中期分析的预设 p 值,也未测试统计显著性(HR=0.754;95% CI:0.584~0.974;p=0.0301)
在内脏转移患者亚组(n=263)中,
阿贝西利+NSAI :65.1 个月,
安慰剂+NSAI : 48.8 个月
⇒即使在被认为预后不良的内脏转移亚组中,使用 abemaciclib 改善 OS 的总体趋势也得以维持(HR=0.708;95% CI:0.508-0.985,p = 0.0392)。
虽然还不能说OS有什么不同,但最终分析的结果是意料之中的。最终的 OS 分析结果定于明年公布,目前 CDK4/6 抑制剂的临床使用没有明确的差异。
然而,这些结果与PALOMA-2 试验的最终 OS 结果不同,该试验在 2022 年 ASCO 年会上公布,并没有证明 OS 存在统计学上的显著差异。亚组分析还显示,阿贝西利的附加作用在内脏转移等预后不良的患者中显着,保持了以往 PFS 和 MONARCH2 OS 结果的特点。包括佐剂中各种 CDK4/6 抑制剂的结果,palbociclib(帕博西尼)和 阿贝西利之间的差异,以前被认为是等效的药物,值得更多考虑。
③acelERA BC和 AMERA-3 试验:口服单药SERD研究结果阴性,但仍值得期待
SERD:是能下调雌激素受体(ER)水平和活性的药物。
氟维司群注射液是一种选择性雌激素受体下调剂(SERD),是现有 SERD 中唯一上市的药物,需要肌肉注射。而目前正在研发的口服SERD有望克服AI治疗过程中出现的与AI耐药相关的ESR1基因突变。(AI治疗,主要是指芳香化酶抑制剂类药物,属于内分泌治疗)
在一项开放标签、随机对照 III 期试验中, Elacestrant(艾拉司群)已被证明对比医生选择的内分泌治疗可改善 PFS 。目前,多家制药公司正在开发口服SERD,此次会议上公布了两项开放标签、随机对照的II期试验结果。
【acelERA BC 试验】
研究纳入了既往接受过1~2线治疗(必须包含内分泌治疗)的ER+/HER2-局部晚期或转移性乳腺癌,将口服 SERD 药物giredestrant 与医师选择的内分泌单药疗法(TPC组)进行了比较。结果,giredestrant 未能显示出 PFS 的显著改善。
★ INV 评估的中位 PFS(中位随访时间为7.89个月),
giredestrant 组:5.6 个月
TPC 组:5.6 个月
风险比为 0.81(95% CI 0.60-1.10,p = 0.1757)
★6 个月 PFS 率
giredestrant 组:46.8%
TPC 组:39.6%
⇒giredestrant 组呈有利趋势。
★ESR1突变阳性患者的中位 PFS
giredestrant 组(51 例患者):5.3 个月
TPC 组(29 例患者):3.5个月
⇒giredestrant 组有利的,但差异不明显(HR=0.60, 95% CI: 0.35-1.03,p = 0.0610)
【AMEERA-3试验】
AMEERA-3是一项随机、开放标签、II期临床试验,旨在评估amcenestrant单药治疗vs医生选择的单药内分泌治疗(包括氟维司群、阿那曲唑、来曲唑、依西美坦以及他莫昔芬)在既往接受过激素治疗的ER+/HER2-局部晚期或转移性乳腺癌患者中疗效和安全性。研究的主要终点是由独立中心审查评估的PFS,研究的次要终点包括总生存期(OS)、客观缓解率(ORR)、疾病控制率(DCR)、临床获益率(CBR)、缓解持续时间(DoR)以及安全性和生活质量评估。
结果,
★中位 PFS
amcenestrant 组:3.6 个月
TPC 组:3.7 个月
⇒没有显着差异(HR=1.051,95% CI:0.789-1.4,p=0.6437),
★ESR1突变阳性患者的中位 PFS
amcenestrant 组:3.7 个月
TPC 组:2.0 个月
⇒没有显着差异(HR=0.9,95% CI;0.565-1.435 , p = 0.6437)
下表总结了上述三种药物的试验结果:
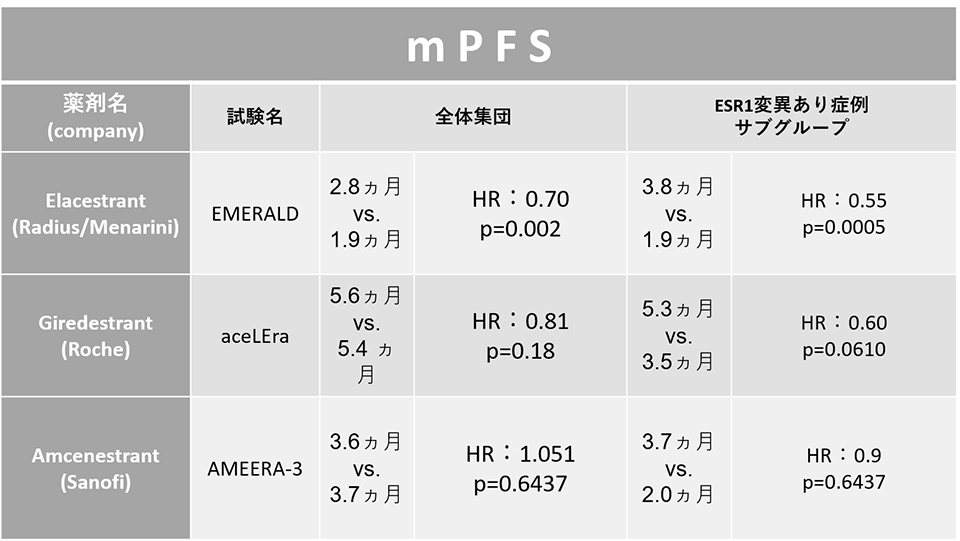
口服SERD的开发目前处于第一线,一些一线治疗III期试验正在进行中,但这些结果给它们蒙上了一层阴影。口服SERD在ESR1突变病例中的疗效一直被认为是合理的。但是,未来,我们将等待目前正在进行的 III 期对比试验的结果,看看它是否真的比现有的 AI 等内分泌疗法和氟维司群更有效。(AMEERA-5 试验已被宣布为阴性试验。)
④DATA 试验:部分患者可能会从延长内分泌治疗中获益
DATA 试验(ClinicalTrials.gov:NCT00301457)是在荷兰进行的一项前瞻性、随机对照、开放标签的Ⅲ期临床试验。旨在研究在他莫昔芬辅助内分泌治疗 2-3 年后未复发的 HR+绝经后乳腺癌患者,延长内分泌治疗的最佳时间等。患者被随机分配接受 3 年的阿那曲唑(833 名)或 6 年的阿那曲唑(827 名)。主要终点为调整的无病生存期(aDFS),定义为随机化3年后的DFS。次要研究终点为调整的总生存期(aOS)。
★10年调整的aDFS率
6年治疗组:69.1%,
3年治疗组:66.0%
⇒HR=0.86,95% CI 0.72-1.01,p = 0.073,差异无统计学意义。
★10 年调整的总生存期(aOS)
6 年治疗组: 80.9%
3 年治疗组:79.2%
⇒HR=0.93,95% CI:0.75-1.16,p = 0.53,未观察到显著差异。
进一步亚组分析显示: 10年调整的aDFS率
★ER +/ PR+
6 年治疗组:70.8%
3 年治疗组:64.4%
HR=0.77,95% CI:0.63-0.93,p=0.018
★淋巴结转移,ER +/ PR+
6 年治疗组: 68.7%
3 年治疗组:60.7%
HR=0.74,95% CI:0.59-0.93,p = 0.011
★肿瘤≥2 cm ,淋巴结转移,ER+/PR+
6 年治疗组: 70.7%
3 年治疗组:66.4%
HR=0.64 , 95% CI .47-0.88, p = 0.005
中位随访 5 年时DFS 没有显著差异。此次最终报告也显示 DFS 结果为阴性。这些亚组的 10 年 aOS 率没有显著改善。
★淋巴结转移,ER +/ PR+
6 年治疗组:81.4%
3 年治疗组:76.7%
HR=0.84,95% CI: 0.63-0.93,p=0.23
★肿瘤≥2 cm ,淋巴结转移,ER+/PR+
6 年治疗组:80.6%
3 年治疗组:72.5%
HR=0.71,95% CI: 0.48-1.05,p=0.084
迄此,5 年内分泌治疗的疗效研究包括 AERAS、MA17、NSABP-B33、NSABP-B42、DATA、GIM4等大型随机对照试验。根据日本乳腺癌学会 2022版诊疗指南的综合分析表明,内分泌治疗 5 年后的 DFS 与 5 年后延长 AI 给药相比有所改善,这一趋势已得到认可。然而,GIM4 研究是唯一显示 OS 改善的随机对照试验,并且延长内分泌治疗在汇总分析中并不显着。
此外,由于现在已知延长AI会增加不良事件,如骨质疏松症的恶化和心血管事件的增加,所以应根据估计的复发基线风险、芳香化酶抑制剂的耐受性和额外的不良事件等因素来综合考虑延长AI。
近年来,研究者们还设计了一些指数来评估芳香化酶抑制剂治疗五年以上的疗效。例如乳腺癌复发指数BCI。它是通过使用FFPE标本,以RT-PCR 为基础的多基因检测方法;还有CTS5评分,它根据肿瘤直径、等级、年龄和淋巴结转移的数量来计算复发风险,对于评估绝经后病例在第五年开始的复发风险很有帮助。这些指标可能有助于筛选出最能延长内分泌治疗中获益的人群。


