癌症病人的恶液质及其治疗
即使不了解癌症恶液质,只是看上去,“恶液质”这个词就会让人毛骨悚然。。眼前浮现的是对晚期癌症患者的常规印象:身体消瘦,面颊凹陷,皮包骨。。
那么,恶液质是必然发生的吗?除了消瘦,还会给肿瘤患者带来什么危害?是不是可以靠吃补回去呢?
首先,我们先来了解一下什么是“恶液质”。
癌症恶液质,指“在正常营养支持下无法完全恢复,导致进行性功能障碍”的状态,被定义为以骨骼肌质量持续减少(无论脂肪是否减少)为特征的多因素综合症。
在进展期癌症患者中可以确认到有80%的患者处于恶液质状态。其中,约20%的患者会因为恶液质所导致的体重和营养流失而死亡。除了体重下降和食欲不振的典型症状外,还有化疗效果减弱,因副作用中断治疗进而影响生存率的。体重减少程度大的癌症患者预后更佳不好,所以,有必要对癌症恶液质进行积极的治疗。
有的患者可能会认为:我只是胃口比较差,导致了体重下降。
这里,我们用下面这张图来解释饥饿和恶液质的区别。
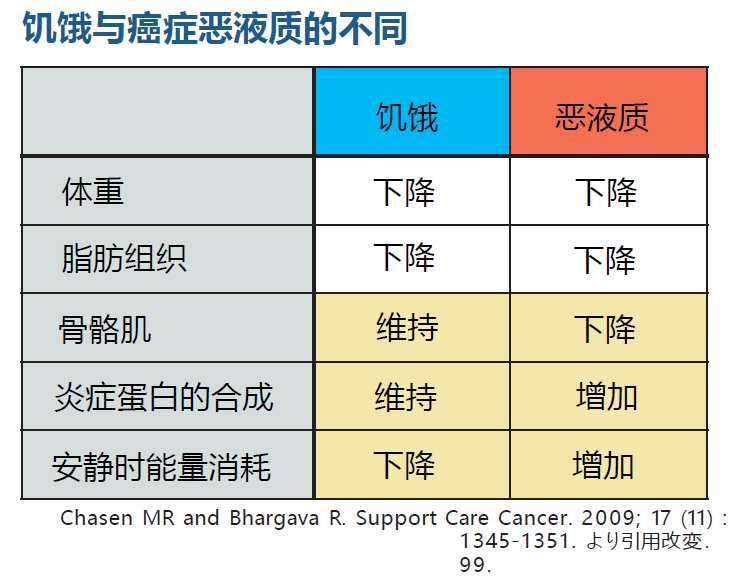
那么,怎样判断癌症患者只是胃口不好导致的消瘦,还是恶液质状态呢?我们一起来看看恶液质的具体症状。
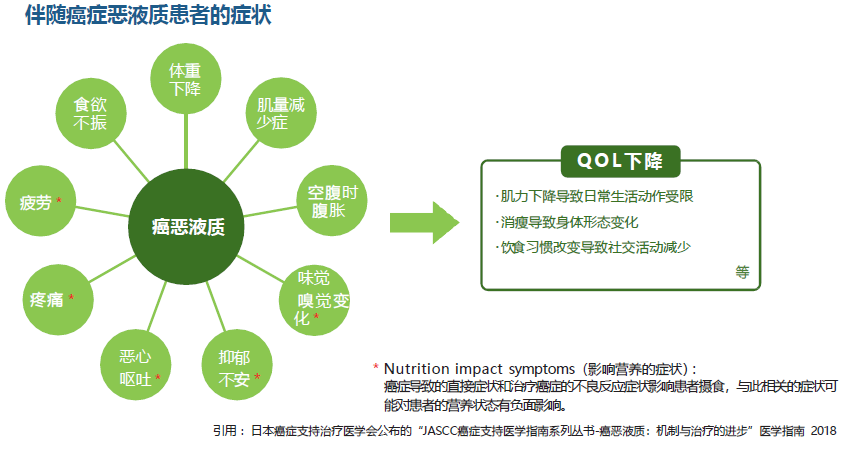
根据患者的主观症状,结合医生对病史的了解和相关必要的检查,如定期监测患者CRP、血糖、白蛋白、胰岛素功能、睾酮等指标有无异常;对患者进行体能测试,包括ECOG、K氏评分、上肢握力测试等,是可以判断出来的。
2011年,欧洲的European Palliative Care Research Collaborative(EPCRC)将癌症的恶液质分为前恶液质、恶液质和不应性恶液质,3个阶段,并提倡以下诊断标准。
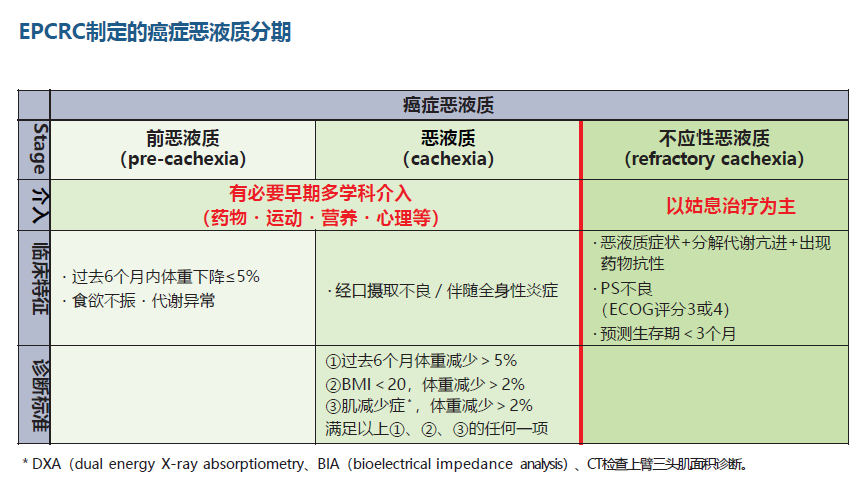
1. 在过去的六个月中,体重减轻了5%以上
2. 体重减轻了2%以上且BMI(Body Mass Index)小于20
3.体重减轻了2%以上且骨骼肌量下降
如果满足这三个条件中的任何一个,并伴有经口摄取营养障碍或全身性炎症的,则可诊断为恶液质。
关于恶液质的治疗,不幸的是,尚不存在标准的治疗方法。现实的治疗策略应考虑多方面的可治疗因素。
1、早期干预+多学科干预
癌症患者体重下降的主要原因是癌症恶液质和饥饿。癌症患者可能同时并存恶液质和饥饿,可治疗的患者比较多。建议早期采取多学科方法介入癌症恶液质的体重下降。
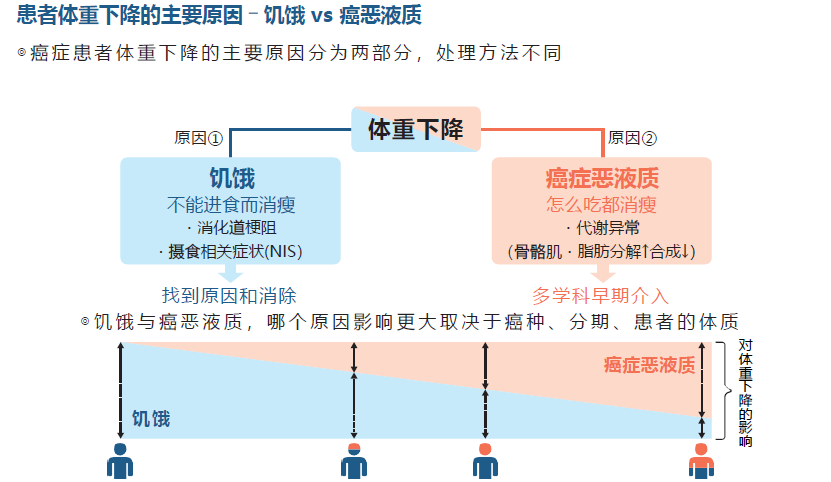
进展阶段的恶液质(不应性恶液质)很难治疗,应该尽早诊断,并在恶液质的早期着手干预治疗。癌症的恶液质以全身型炎症为背景,复杂原因相关,表现为食欲不振、骨骼肌减少、肝脏、脂肪组织代谢变化等。因此癌症恶液质的治疗除了药物疗法,还需要营养疗法、运动疗法、以及心理、社会的干预。
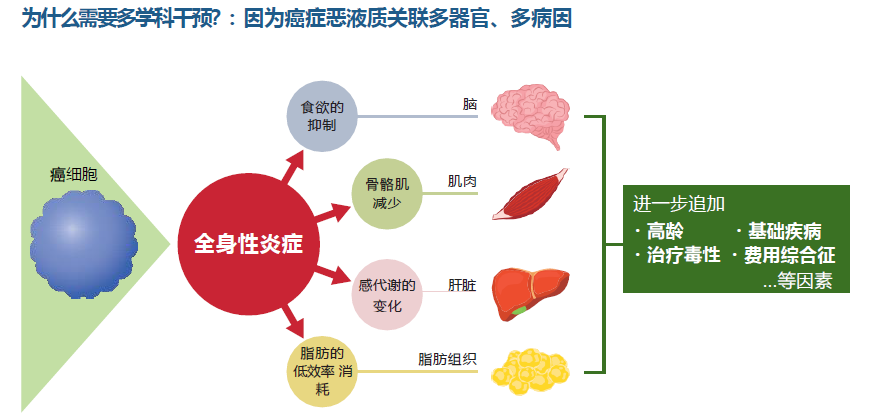
2、药物治疗
药物治疗需要再医生的建议下实施,可用的药物包括:促进食欲的药物,促进胃动力的药物,甾体激素,非甾体抗炎药等。然而这些药物的治疗证据都不充分。
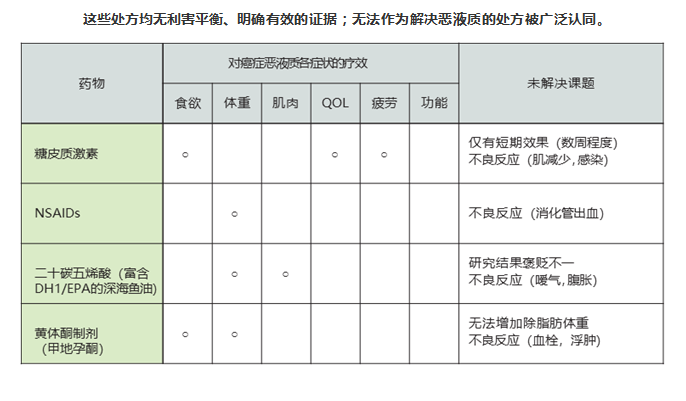
癌症恶液质“无药可救”的状态直到2021年4月发生了变化。
日本小野制药宣布在日本推出 【エドルミズ錠50mg】Adlumiz(anamorelin)50mg 片剂(口服药物),用于治疗非小细胞肺癌、胃癌、胰腺癌、结直肠癌等恶性肿瘤患者的癌症恶病质(cancer cachexia)。临床数据显示,Adlumiz在癌症恶病质患者中具有增加体重、肌肉质量、食欲的作用。
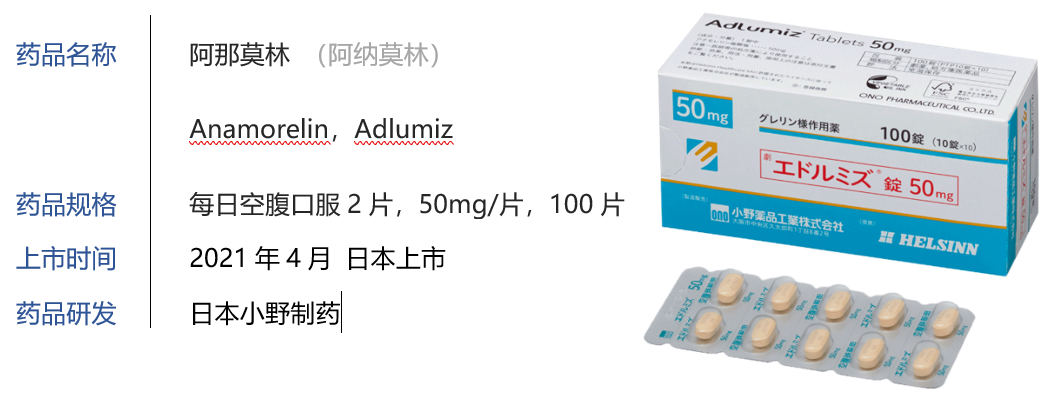
3、非药物治疗
单独药物疗法无法获得充分的疗效,有必要与营养疗法和运动疗法组合使用。
营养治疗
营养支持不仅可以增加患者能量及各种营养素的摄入,改善患者营养状况,还可以调节肿瘤患者的异常代谢,有益于抗肿瘤治疗。
营养治疗包括肠内营养(EN)和肠外营养(PN)两种方式,欧洲癌症恶液质临床治疗指南推荐首选肠内营养。
体育锻炼
对各期恶液质患者,除营养支持外的非药物治疗,目前还推荐包括鼓励适当锻炼、心理干预等措施进行辅助治疗。
运动可以增加胰岛素的敏感性,提高蛋白合成效率,提高患者的身体功能,改善代谢模式,保持肌肉含量。外科临床营养(ESPEN)指南中,将运动干预作为A类推荐(基本上没有禁忌证就可以使用),根据患者的自身特点,定制个体化运动方案。
体育锻炼方面建议每周不少于5次,每日30~50分钟的中等强度运动,以出汗为好。即使是卧床患者也建议进行适合的运动(包括手、腿、头颈部及躯干的活动)。肌肉减少的老年患者提倡抗阻运动。
恶液质的治疗,需要多学科联合治疗方案的制定和开展。最需要的,是患者和家属能够重视营养治疗,关注患者的体重变化,及早预防恶液质,才是治疗的最好办法。


